西奥罗尼是公司独家发现的、具有全球专利保护的新分子实体,机制新颖,为三通路肿瘤靶向抑制剂。西奥罗尼选择性抑制Aurora B、CSF1R和VEGFR/PDGFR/c-Kit等肿瘤发生发展相关蛋白激酶靶点,在抑制肿瘤细胞增殖、抗肿瘤新生血管生成、调控肿瘤免疫微环境等环节发挥多方位广谱的抗肿瘤作用,已在末线肿瘤单药治疗的临床试验中展现良好疗效和安全性。
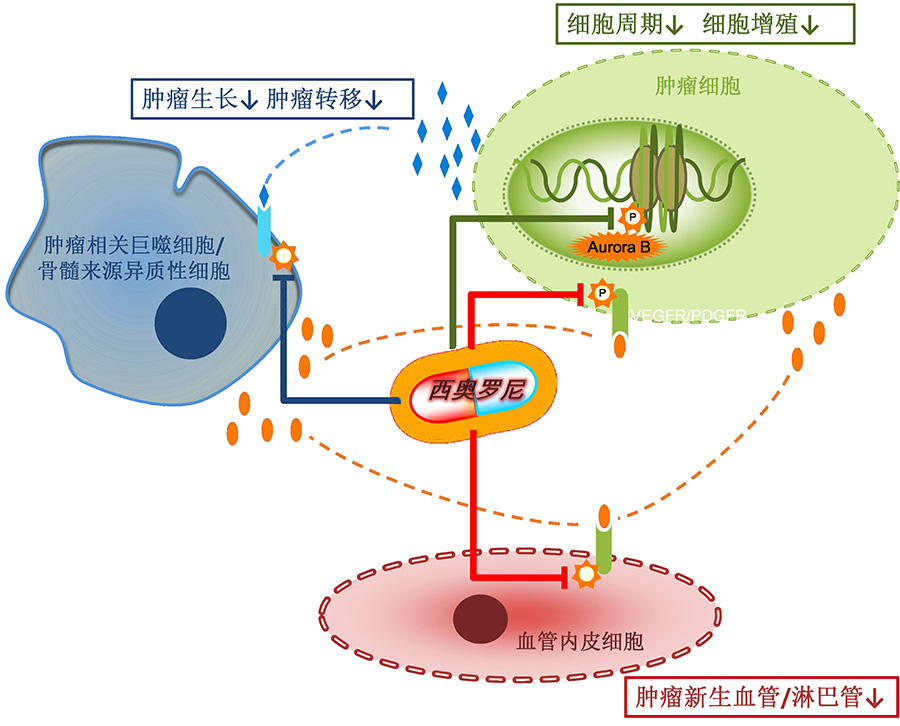
图 西奥罗尼抗肿瘤三通路机理示意图
全球范围在研适应症情况:
√ 西奥罗尼联合白蛋白紫杉醇和吉西他滨一线治疗胰腺导管腺癌患者的II期临床试验已完成入组。截至中位随访9.6个月时,西奥罗尼联合方案ORR(客观缓解率)达到50%,约半数患者仍在持续用药中,mPFS(中位无进展生存期)为9.1个月(95%CI:6.2-10.9),OS(总生存期)数据尚未成熟。该试验疗效明显优于化疗历史数据,且患者的安全性和耐受性良好。
√ 2026年1月,西奥罗尼联合特瑞普利单抗及白蛋白紫杉醇和吉西他滨一线治疗转移性胰腺导管腺癌患者的III期临床研究获得NMPA批准。
√ 西奥罗尼联合紫杉醇治疗铂难治或铂耐药复发卵巢癌患者的随机、双盲、对照、多中心III期临床试验正在进行。
√ 西奥罗尼美国Ib/II期正在进行110mg剂量爬坡,尚未观察到剂量限制性毒性(DLT)。