November 03,2025
2025年欧洲肿瘤内科学会年会(ESMO)于10月17日至21日在德国柏林以线上结合线下的形式举行。中山大学肿瘤防治中心张星教授团队最新研究成果在此次ESMO年会上以口头报告形式公布。该研究[1]是一项西达本胺联合特瑞普利单抗治疗晚期软组织肉瘤的单臂、开放、多中心Ⅱ期临床试验。本次公布的数据显示,客观缓解率(ORR)达30.4%,疾病控制率(DCR)为73.9%,中位无进展生存期(mPFS)为7.1个月;其中,在高分化/去分化脂肪肉瘤(WDLPS/DDLPS)这一传统上对化疗和免疫治疗敏感性有限的亚型中,取得了显著的疗效(ORR 62.5%,mPFS 17.1个月),提示西达本胺联合特瑞普利单抗为无标准治疗/标准治疗失败后晚期软组织肉瘤患者尤其是 WDLPS/DDLPS 患者带来新的治疗选择,有望成为未来治疗此类疾病的重要策略之一。
两难之境:晚期软组织肉瘤治疗选择匮乏,免疫单药难破“疗效僵局”
肉瘤是一类起源于间叶组织(如骨、肌肉、脂肪等)的罕见恶性肿瘤,约占成人恶性肿瘤的1%,其组织学亚型超过百种,主要包括软组织肉瘤(STS)及骨肉瘤等,生物学行为及临床表现差异大。尽管早期患者可通过手术获得治愈,仍有约30–40%的患者会发生转移。晚期肉瘤预后差,5年生存率低于30%,治疗面临巨大挑战[2]。当前,晚期肉瘤的一线标准治疗以多柔比星单药为基础,但疗效有限,ORR 通常仅5%-17%,中位总生存期约8–15个月[3]。二线及后线治疗选择更少,常用药物包括吉西他滨、曲贝替定等,缓解率低,患者生存获益有限[4]。因此,晚期肉瘤患者存在迫切的未满足临床需求。近年来,PD-1/PD-L1抑制剂在多种实体瘤中取得显著进展,但在肉瘤中总体疗效欠佳,仅少数亚型(如未分化多形性肉瘤、腺泡状软组织肉瘤)显示一定敏感性[5]。多数肉瘤为“免疫冷肿瘤”,表现为T细胞浸润不足及免疫抑制微环境,这可能限制了免疫单药疗效[6]。
破局之道:西达本胺联合PD-1抑制剂,为“冷肿瘤”注入活力
组蛋白去乙酰化酶抑制剂(HDACi)西达本胺,可通过表观遗传调控增强肿瘤免疫原性,改善免疫微环境,为联合PD-1抑制剂提供理论依据[7]。临床前研究显示,HDAC抑制剂与免疫检查点抑制剂具有协同抗肿瘤效应[7-8]。基于此,研究团队设计了一项Ⅱ期临床试验,首次系统评估该联合方案在晚期肉瘤患者中的疗效与安全性,有望为晚期肉瘤提供新的治疗方向。
精准聚焦:研究设计的关键要素与患者基线特征剖析[1]
这是一项单臂、开放、多中心Ⅱ期临床试验,共纳入69例可评估疗效的无标准治疗或标准治疗失败后的晚期肉瘤患者。关键排除标准包括既往接受过HDAC抑制剂或免疫检查点抑制剂治疗。所有入组患者接受西达本胺(30mg,口服,每周两次)联合特瑞普利单抗(240mg,静脉输注,每21天一次)的治疗方案,直至疾病进展或出现不可耐受的毒性反应。研究的主要终点为根据RECIST 1.1标准评估的 ORR 。次要终点包括 PFS 、总生存期(OS)、 DCR 和安全性(根据CTCAE V5标准评估)。

图1 研究设计
入组患者基线特征如下表1所示,患者中位年龄47岁,中位既往治疗线数为2线。主要的病理亚型包括平滑肌肉瘤(29%)、高分化/去分化脂肪肉瘤(34.8%)、未分化肉瘤(7.2%)、黏液样/圆细胞脂肪肉瘤(5.8%)和骨肉瘤(4.3%)。
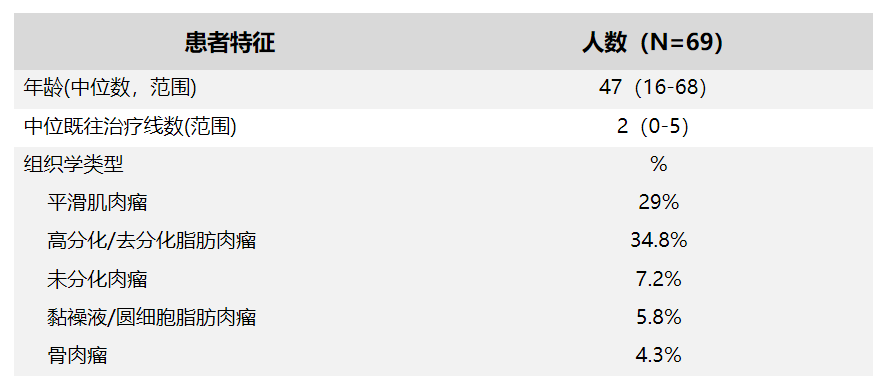
表1 入组患者基线特征
数据洞察:疗效与安全性数据的全面剖析[1]
在69例可评估疗效的患者中, ORR 为30.4%(21例), DCR 为73.9%(51例)。患者获得初始反应的中位时间为5个月(95% CI 3-7)。中位 PFS 为7.1个月(95% CI 4.0-10.2)。亚组分析结果:WDLPS/DDLPS 患者疗效显著优于其他亚型疗效,WDLPS/DDLPS患者的ORR高达62.5%(15/24),而其他亚型患者仅为13.3%(6/45),差异具有极显著的统计学意义(P<0.001)。相应地,WDLPS/DDLPS患者的中位PFS也显著延长至17.1个月,远高于其他亚型患者的3.6个月(P<0.001)。安全性方面,联合治疗总体耐受性良好。大多数不良事件为1-2级,主要包括贫血(55.1%)、甲状腺功能减退(44.9%)、白细胞减少(33.3%)、血小板减少(30.4%)、中性粒细胞减少(24.6%)、恶心/呕吐(24.6%)和乏力(15.9%)。3-4级不良事件中,最常见的是中性粒细胞减少(27.5%)、血小板减少(23.2%)、白细胞减少(14.5%)、恶心/呕吐(10.1%)和贫血(1.4%)。
大咖视角:张星教授解读研究价值与未来方向
张星教授:晚期肉瘤治疗因其高度异质性和对传统化疗的耐药性,始终是临床实践中的难点。对于无标准治疗或标准治疗失败后的患者,选择匮乏,预后极差,存在迫切的未满足需求。尽管免疫检查点抑制剂为部分瘤种带来了变革,但在肉瘤中,除极少数特殊亚型外,单药疗效有限[5]。因此,如何通过联合用药策略逆转免疫抑制微环境、将“冷肿瘤”转化为“热肿瘤”,成为当前的研究热点。
HDAC抑制剂在这一领域展现出较大的潜力。西达本胺作为我国自主研发的新型、亚型选择性HDAC抑制剂,其具有抗肿瘤及增强免疫的作用。此前的研究已为其免疫调控作用提供了扎实的基础。例如,在淋巴瘤领域,西达本胺已被证实能上调肿瘤细胞表面MHC和共刺激分子表达,增强抗原呈递[9];在实体瘤临床前研究中,它也显示出可抑制调节性T细胞功能、促进细胞毒性T细胞浸润等免疫调节作用[10]。这些机制共同奠定了西达本胺与PD-1抑制剂联合的理论基础,即通过表观遗传调控解除免疫抑制,从而增强免疫治疗的疗效。我们团队此前报告了该项II期研究的中期分析结果,已初步验证了西达本胺联合特瑞普利单抗在晚期肉瘤中的潜力[11]。本次ESMO大会上公布的是最新分析结果,该分析基于更长时间的随访和完整人群,将进一步表明该联合方案的可行性。结果显示,西达本胺联合特瑞普利单抗在经治晚期肉瘤患者中安全性良好,且疗效显著,整体ORR达30.4%,DCR为73.9%,mPFS为7.1个月。更值得关注的是,该联合方案在WDLPS/DDLPS这一传统上对化疗和免疫治疗均不敏感的亚型中,取得了突破性的疗效(ORR 62.5%,mPFS 17.1个月)。这一数据远超现有二线及后线治疗的历史数据[12-13],提示该组合可能激发了这一特定亚型的治疗潜力,期待进一步的探索和真实世界研究的验证。
参考文献:
[1]2025 ESMO, abstract 2689MO.
[2] Gamboa AC,et al. CA Cancer J Clin. 2020;70(3):200-229.
[3] Tian Z, Yao W.Front Pharmacol. 2023;14:1199292. Published 2023 Aug 11.
[4] Schöffski P, et al. Lancet. 2016;387(10028):1629-1637.
[5.]Tawbi HA, et al. Lancet Oncol. 2017;18(11):1493-1501.
[6] D'Angelo SP, et al. Hum Pathol. 2015;46(3):357-365.
[7] Woods DM, et al. Cancer Immunol Res. 2015;3(12):1375-1385.
[8] Terranova-Barberio M, et al. Oncotarget. 2017;8(69):114156-114172. Published 2017 Dec 12.
[9.]Shi Y, et al. Ann Oncol. 2015.
[10] Wang L, et al. Oncologist. 2025;30(7):oyaf155.
[11] Xing Zhang et al. JCO 41, 11566-11566(2023).
12. Dickson MA, et al. JAMA Oncol. 2016;2(7):937-940.
13.D'Angelo SP, et al. Lancet Oncol. 2018;19(3):416-426.